

根据药渡数据统计分析,本次统计周期(2024.10.12-10.18)全球(不含中国)共有6个新药获批上市。其中,BLA批准2个,新适应症批准4个。与上个统计周期相比,本次增加2个批准新药。10月15日,君实生物宣布抗PD-1单抗药物特瑞普利单抗的上市申请已先后在印度和中国香港获批上市,用于复发/转移性鼻咽癌的治疗。此次获批的适应症分别为:1)特瑞普利单抗联合顺铂/吉西他滨作为转移性或复发性局部晚期鼻咽癌成人患者的一线治疗;2)特瑞普利单抗单药治疗既往含铂治疗过程中或治疗后疾病进展的复发性、不可切除或转移性鼻咽癌的成人患者。研究结果显示,特瑞普利单抗联合化疗使患者的疾病进展风险降低48%,死亡风险降低37%,PFS对比单纯化疗延长了13.2个月。10月18日,德琪医药宣布,MFDS已批准希维奥®(塞利尼索片)的补充新药上市申请,联合硼替佐米和地塞米松用于治疗至少接受过一种先前治疗的多发性骨髓瘤成人患者。塞利尼索片是一款全新机制的口服选择性核输出蛋白(XPO1)抑制剂。通过抑制核输出蛋白XPO1,该产品可促使肿瘤抑制蛋白和其他生长调节蛋白的核内储留和活化,并下调细胞浆内多种致癌蛋白水平。全球(不含中国)新药批准情况(部分)


根据药渡数据统计分析,本次统计周期(2024.10.12-10.18)全球(不含中国)共有10个新药申报上市。其中,NDA申报8个,BLA申报2个。与上次统计周期相比,本次增加4个NDA/BLA申报。10月15日,恒瑞医药公告称其重新提交的注射用卡瑞利珠单抗联合甲磺酸阿帕替尼片用于不可切除或转移性肝细胞癌患者的一线治疗的BLA获得FDA受理。研究结果显示,此疗法具有显著的生存获益和可耐受的安全性,中位PFS为5.6个月,中位OS达到23.8个月。
根据药渡数据统计分析,本次统计周期(2024.10.12-10.18)全球(不含中国)共有4个药物获监管机构特殊资格认定。其中,化学药2个,生物药1个,疫苗1个。与上次统计周期相比,本次减少2个获监管机构特殊资格认定的药物。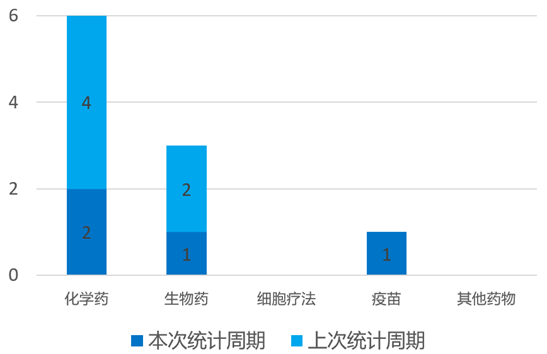
10月15日,Immuneering宣布FDA已授予IMM-1-104孤儿药资格认定,用于治疗胰腺癌。IMM-1-104旨在通过每日一次给药对MAPK通路的深度循环抑制,实现普遍的RAS活性,即选择性地影响癌细胞。IMM-1-104目前正在晚期实体瘤(包括胰腺癌)患者中进行IIa期临床试验,其中最近报道了联合改良吉西他滨/白蛋白结合型紫杉醇治疗的一线胰腺癌患者的阳性初始反应数据。10月16日,Theriva Biologics宣布EMA已授予VCN-01孤儿药产品资格,用于治疗视网膜母细胞瘤。VCN-01是一种全身给药的溶瘤腺病毒,旨在选择性和侵袭性地在肿瘤细胞内复制并降解肿瘤基质。这种独特的作用方式使VCN-01能够通过以下方式发挥多种抗肿瘤作用:(i)选择性感染和裂解肿瘤细胞;(ii)加强联合给药化疗产品的可及性和灌注;(iii)增加肿瘤免疫原性并使肿瘤暴露于患者的免疫系统和联合给药的免疫治疗产品。全身给药使VCN-01能够对原发肿瘤和转移瘤发挥作用。特殊资格认定情况(部分)

根据药渡数据统计分析,本次统计周期(2024.10.12-10.18)全球(不含中国)新药临床研发状态更新共计46条,涉及肿瘤、血液和淋巴疾病、遗传代谢病、神经疾病以及免疫系统疾病等共计13个领域。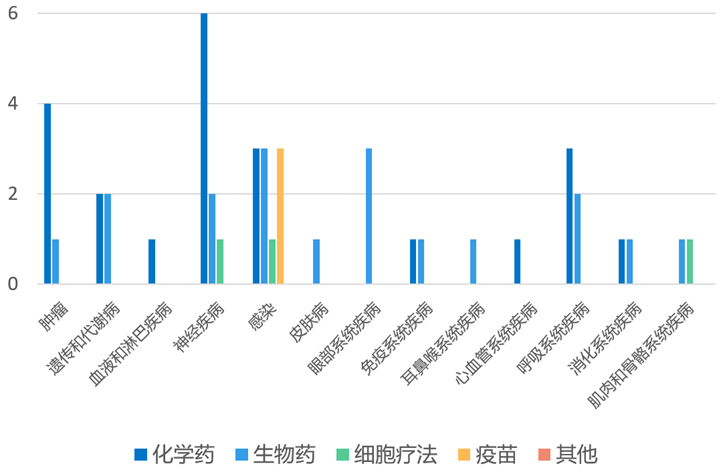
其中,感染领域临床进展更新居各领域之首,为10条:涉及化学药3条,生物药3条,细胞疗法2条。10月15日,Celltrion公布了皮下注射英夫利昔单抗(CT-P13 SC)的2年事后分析结果,强调剂量递增是管理炎症性肠病反应丧失的一种选择。分析表明,对于最初有反应但随后失去反应的患者,静脉内(IV)诱导后CT-P13 SC的剂量递增在102周的延长时间内显示出临床疗效,患者UC的平均改良Mayo评分和CD的平均CDAI评分具有统计学意义降低。10月16日,长春高新发布公告称,其子公司金赛药业GenSci122片项目获得FDA新药临床试验默示许可。GenSci122是具有新型结构的小分子KIF18A抑制剂,KIF18A抑制剂与染色体不稳定(CIN)及全基因组加倍(WGD)+构成合成致死。与正常二倍体细胞相比,KIF18A在CIN肿瘤细胞中高表达,具有CIN特性的肿瘤细胞对KIF18A具有依赖性。靶向抑制KIF18A可作为肿瘤的潜在治疗策略,同时不会显著影响正常二倍体细胞的增殖。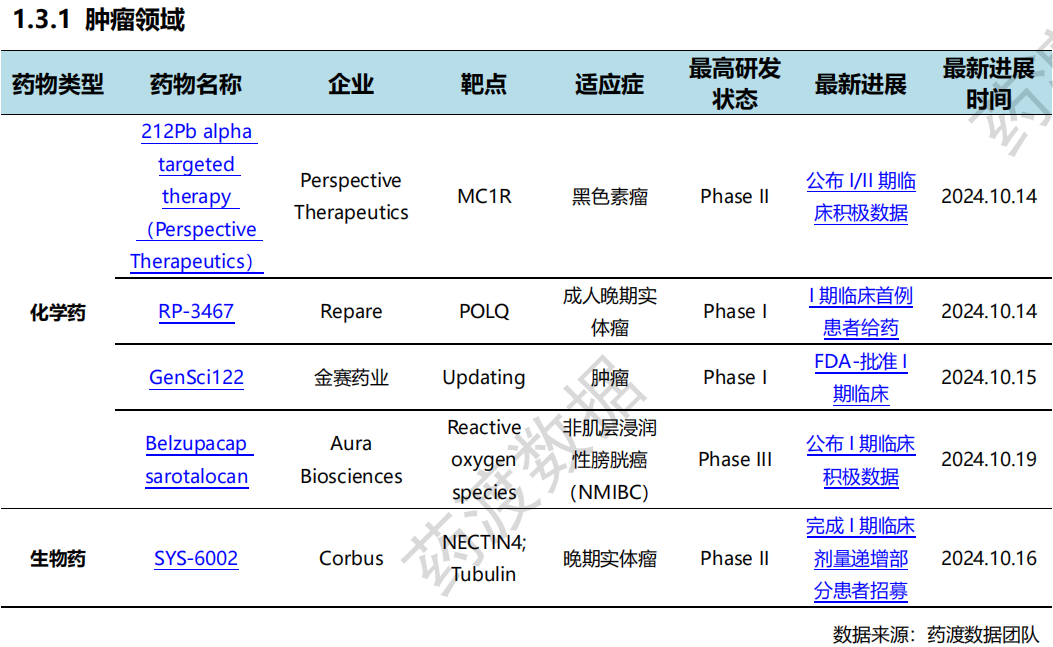


本次统计周期(2024.10.12-10.18)全球(含中国)医药交易时间共计33起,涉及药物权益转让、公司并购等多起交易事件。
全球医药交易时间汇总表(部分)

根据药渡数据统计分析,本次统计周期(2024.10.12-10.18)国内共有4个新药获NMPA批准上市。其中,BLA批准1个,新适应症批准3个。与上次统计周期相比,本次减少4个NMPA批准新药。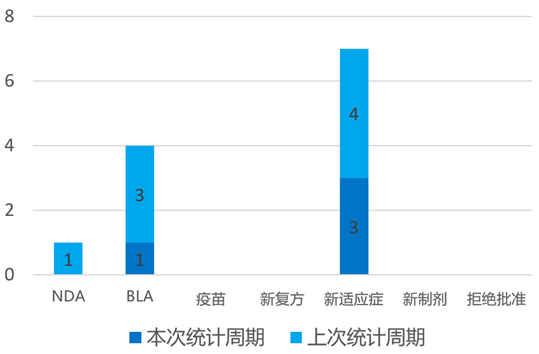
10月14日,NMPA官网公示,Roche的法瑞西单抗(Faricimab)注射液新适应症上市申请获得批准,用于治疗视网膜中央静脉阻塞(CRVO)继发黄斑水肿。法瑞西单抗可同时靶向阻断两条致病关键通路,在原有抑制新生血管生成的基础上同时提高血管稳定性,降低血管异常渗漏,改善患者的视力。研究表明,对于由CRVO引起的黄斑水肿患者,每4周接受法瑞西单抗注射(长达24周)视力获得具有非劣效性,从基线到第24周,法瑞西单抗能使患者的视网膜液迅速干燥。10月14日,NMPA官网公示由Daiichi Sankyo申报的注射用德曲妥珠单抗(Enhertu)已经获得上市批准,用于治疗存在HER2激活突变且既往接受过至少一种系统治疗的不可切除或转移性成人非小细胞肺癌(NSCLC)患者。研究结果显示,在既往经治HER2突变NSCLC中国患者中实现ORR近60%,DCR超过91%,多个疗效指标显示德曲妥珠单抗带来了具有临床意义和持久的缓解,而且安全性可控。
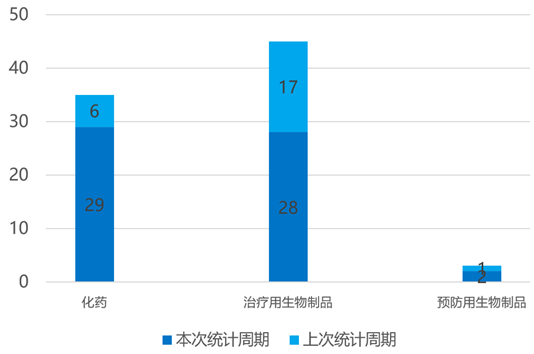
根据药渡数据统计分析,本次统计周期(2024.10.12-10.18)国内共有59个新药获临床默示许可,涉及100个受理号。其中,化学药29个,治疗用生物制品28个,预防用生物制品2个。与上次统计周期相比,本次增加66个临床默示许可获批受理号。
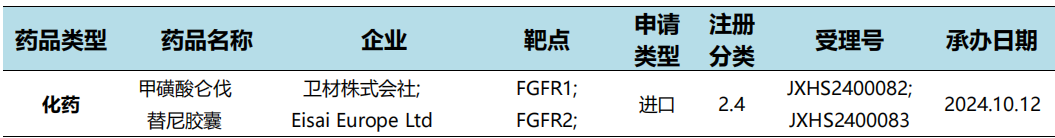
本周国内新药临床默示许可进展(部分)

根据药渡数据统计分析,本次统计周期(2024.10.12-10.18)国内共有18个新药申报上市,涉及29个受理号。其中,化药8个,治疗用生物制品8个,预防用生物制品2个。与上个统计周期相比,本次增加9个新药申报上市受理号。

根据药渡数据统计分析,本次统计周期(2024.10.12-10.18)国内共有67个新药申报临床,涉及100个受理号。其中,化学药36个,治疗用生物制品30个,预防用生物制品1个。与上次统计周期相比,本次增加69个临床申报受理号。


根据药渡数据统计分析,本次统计周期(2024.10.12-10.18)国内共有4个药物获NMPA特殊资格认定。其中,化学药1个,生物药2个,疫苗1个。与上次统计周期相比,本次增加3个获监管机构特殊资格认定的药物。10月15日,NMPA药品审评中心官网最新公示,和其瑞医药申报的1类新药HMI-115拟纳入突破性治疗品种,适应症为治疗子宫内膜异位症相关的中重度疼痛。HMI-115是一款靶向泌乳素受体(PRLR)的单抗新药,PRLR表达失调可能与子宫内膜异位症的发病机制有关,而靶向催乳素和催乳素受体的药物可能改善和控制该疾病相关的疼痛。研究公示信息显示,HMI-115的给药方式为皮下给药,只需每2周一次,共6个治疗周期。同日,NMPA药品审评中心官网公示南京远大赛威信生物医药有限公司申报的1类新药TVAX-008注射液拟纳入突破性治疗品种,适用于治疗慢性乙型肝炎病毒(HBV)感染。TVAX-008利用多靶点乙肝表面抗原(HBsAg)和HBcAg联合CpG寡聚脱氧核苷酸佐剂,其中HBsAg/HBcAg促进体液免疫,恢复Th1/Th2平衡;CpG激活B细胞和pDC的TLR9,诱导针对乙肝病毒的细胞免疫。该产品可通过不同途径呈递乙肝抗原,打破机体的免疫耐受,有效诱导免疫应答,从而达到治疗和控制慢性乙肝感染的效果。
根据药渡数据统计分析,本次统计周期(2024.10.12-10.18)国内新药临床研发状态更新共计4条,涉及肿瘤、消化系统、遗传和代谢疾病以及皮肤病共计4个领域。其中,化学药1条,生物药3条。与上次统计周期相比,本次减少2条国内新药临床研发状态更新。
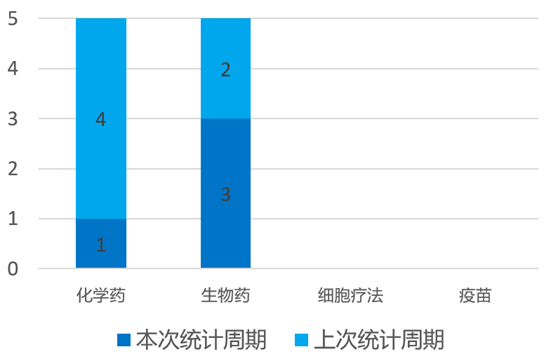
10月13日,博瑞医药宣布BGM0504在非糖尿病的超重或肥胖受试者中开展的II期临床试验,达到主要终点和关键次要终点。BGM0504是一款靶向胰高血糖素样肽1(GLP-1)和葡萄糖依赖性促胰岛素多肽(GIP)受体双重激动剂,每周给药一次。非糖尿病24周平均减重18.5%和减腰围13.4cm,并显著降低多项心血管代谢风险指标,增加胰岛素敏感性,耐受性和安全性良好。10月17日,信达生物宣布匹康奇拜单抗(IL-23p19抗体)治疗溃疡性结肠炎的II期临床研究达成主要终点:诱导治疗期第12周时,匹康奇拜单抗200mg组和600mg组达到临床缓解的受试者比例分别是20.0%和14.0%,达到临床应答的受试者分别为54.0%和68.0%,达到症状缓解、内镜缓解或黏膜愈合的受试者比例均高于安慰剂组,总体安全性良好。
关于公开征求《放射性治疗药物申报上市临床风险管理计划技术指导原则(征求意见稿)》意见的通知为进一步指导放射性治疗药物申报上市时的风险管理,我中心组织起草了《放射性治疗药物申报上市临床风险管理计划技术指导原则(征求意见稿)》。我们诚挚地欢迎社会各界对征求意见稿提出宝贵意见和建议,并及时反馈给我们,以便后续完善。征求意见时限为自发布之日起1个月。翰森制药「熬出头了」
2019年之前,翰森制药还是一家以仿制药为主的传统制药企业,仿制药业务收入和利润增速的放缓,让其下定决心转型创新药。然而,创新转型并非一帆风顺。2022年,翰森制药创新药数量从2019年之前的1款增加到7款,创新药收入占比也首次超过了仿制药,达到了50.6%,但也就是在这一年,翰森制药营收和净利润首次出现负增长。直到2024年中报业绩出炉,营收65.06亿元,同比增长44.21%,净利润27.26亿元,同比增长111.47%,创新药收入占比高达77.34%。一切质疑烟消云散,翰森制药进化到了势不可挡的阶段。更多资讯,请阅读原文随着双抗出海升温,研发管线以双抗为主的宜明昂科-B,股价自9月12日以来累计涨幅高达约100%。资本市场的加持,加之双抗管线达成大额BD交易,下一代Biotech龙头正在浮出水面。对于带“B”标签的Biotech,投资者最关心的问题就是:什么时候能实现扭亏为盈?随着越来越多Biotech凭借管线出海实现盈利,宜明昂科也紧跟这一趋势,达成了大额BD交易。更多资讯,请阅读原文为方便读者阅读及保存,我们将周报原文整理成了PDF版本,如需获取全文,可点击最上方蓝字,在药渡Daily公众号后台回复“1024创新药周报”,即可下载。



