国家癌症中心最新发布的数据显示,我国胃癌的年发病人数超过35万,位列所有恶性肿瘤第5位;死亡人数超过26万人,位列恶性肿瘤第3位。我国胃癌患者大约占全球40%——这意味着,我每天有近千人被确诊为胃癌。更严峻的是,大部分患者确诊时已到晚期,错过最佳治疗窗口。
在2025年美国临床肿瘤学会(ASCO)年会上,中国学者在胃癌治疗领域展示了多项数据,尤其是抗体药物及其联合治疗方案的研究成果备受瞩目。近年来,随着免疫治疗、靶向治疗等新兴疗法的不断发展,胃癌的治疗格局正在发生深刻变革。本次ASCO会议上,中国研究团队展示的多项创新性抗体药物的研究成果,不仅涵盖了HER2、CLDN18.2等经典靶点,还探索了新兴靶点如TROP-2、STEAP1等的应用潜力。这些研究不仅为胃癌患者带来了新的治疗希望,也为全球胃癌治疗领域提供了重要的参考和借鉴。
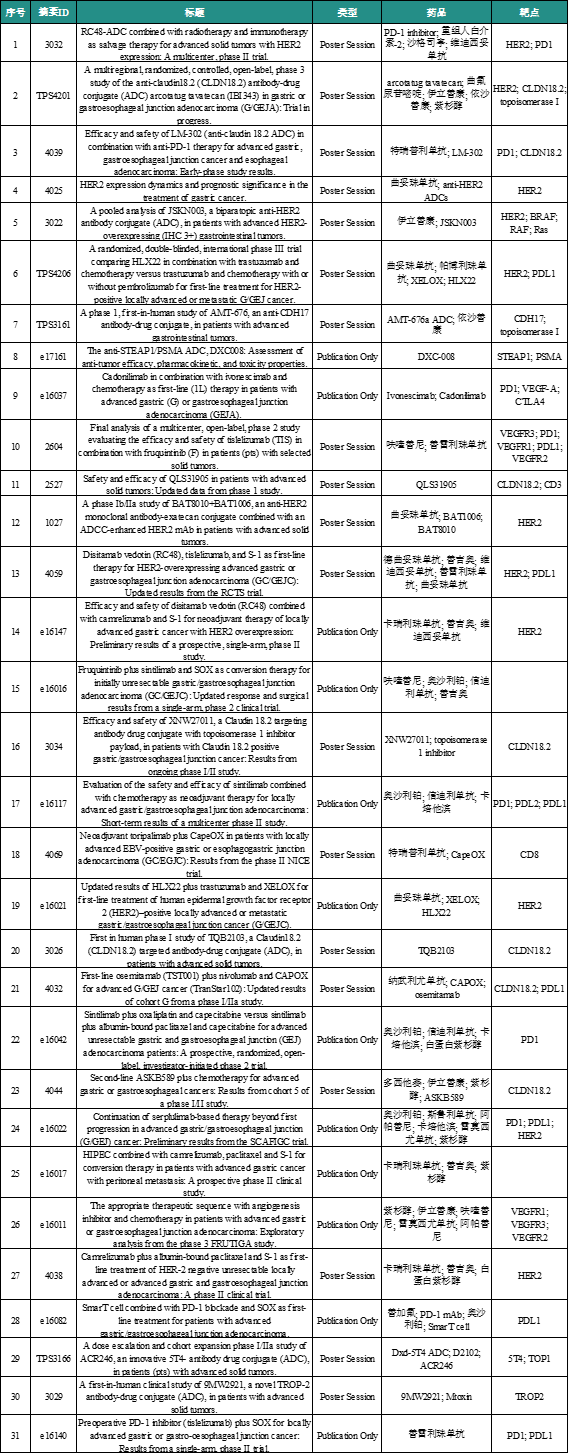
2025ASCO中国胃癌抗体类摘要汇总
RC48-ADC combined with radiotherapy and immunotherapy as salvage therapy for advanced solid tumors with HER2 expression: A multicenter, phase II trial.

概述:该多中心Ⅱ期试验旨在评估RC48-ADC联合放疗和免疫治疗在HER2表达的晚期实体瘤患者中的疗效和安全性。研究纳入了52名患者,包括妇科肿瘤、胰腺癌和胃癌等。结果显示,总体客观反应率(ORR)为36.5%,中位无进展生存期(PFS)为5.9个月,中位总生存期(OS)为14.3个月。治疗相关不良事件大多为轻度。研究结论表明,这种联合疗法在HER2表达的晚期实体瘤患者中显示出良好的疗效和可管理的安全性,有望成为一种有效的挽救治疗选择。
A multiregional, randomized, controlled, open-label, phase 3 study of the anti-claudin18.2 (CLDN18.2) antibody-drug conjugate (ADC) arcotatug tavatecan (IBI343) in gastric or gastroesophageal junction adenocarcinoma (G/GEJA): Trial in progress.

概述:这项多区域、随机、对照、开放标签的Ⅲ期研究旨在评估抗CLDN18.2抗体药物偶联物(ADC)arcotatug tavatecan(IBI343)在胃或胃食管交界腺癌(G/GEJA)患者中的疗效和安全性。研究计划纳入450名患者,主要纳入标准包括局部晚期不可切除或转移性G/GEJA、CLDN18.2阳性(IHC膜染色强度≥2+,≥75%肿瘤细胞)等。主要终点为无进展生存期(PFS)和总生存期(OS)。研究正在进行中,旨在为CLDN18.2阳性G/GEJA患者提供新的治疗选择。
fficacy and safety of LM-302 (anti-claudin 18.2 ADC) in combination with anti-PD-1 therapy for advanced gastric, gastroesophageal junction cancer and esophageal adenocarcinoma: Early-phase study results.

概述:该早期研究评估了抗CLDN18.2 ADC(LM-302)联合抗PD-1疗法(toripalimab)作为一线治疗方案在晚期胃癌、胃食管交界癌和食管腺癌患者中的疗效和安全性。研究纳入了43名患者,结果显示联合治疗的客观反应率(ORR)为65.9%,疾病控制率(DCR)为85.4%。在CLDN18.2高表达(IHC 2+/3+)的胃癌患者中,ORR为71.9%。研究结论表明,LM-302联合toripalimab在CLDN18.2阳性患者中显示出良好的抗肿瘤活性和可管理的安全性,支持进一步开展大规模临床试验。
HER2 expression dynamics and prognostic significance in the treatment of gastric cancer.

概述:该研究探讨了胃癌治疗过程中HER2表达的变化及其对预后的影响。研究纳入了274名胃癌患者,分析了治疗前后HER2免疫组化(IHC)结果。结果显示,HER2表达变化率为42.7%,低一致性(Kappa=0.179)。在接受抗HER2治疗的患者中,HER2表达变化率更高,主要表现为HER2减少。研究结论表明,HER2表达在胃癌治疗过程中频繁变化,尤其在免疫治疗和靶向治疗后,与较差的生存结果相关,动态HER2检测有助于指导胃癌的精准治疗。
A pooled analysis of JSKN003, a biparatopic anti-HER2 antibody conjugate (ADC), in patients with advanced HER2-overexpressing (IHC 3+) gastrointestinal tumors.

概述:该研究对JSKN003(一种双特异性抗HER2抗体药物偶联物)在HER2过表达(IHC 3+)胃肠道肿瘤患者中的疗效和安全性进行了汇总分析。研究纳入了40名患者,结果显示,整体客观反应率(ORR)为66.7%,疾病控制率(DCR)为94.7%。在胃癌/胃食管交界癌患者中,ORR为68.2%,中位无进展生存期(PFS)为9.59个月。研究结论表明,JSKN003在经多线治疗的患者中显示出良好的抗肿瘤活性和可管理的安全性,支持其进一步开发。
A randomized, double-blinded, international phase III trial comparing HLX22 in combination with trastuzumab and chemotherapy versus trastuzumab and chemotherapy with or without pembrolizumab for first-line treatment for HER2-positive locally advanced or metastatic G/GEJ cancer.

概述:该国际Ⅲ期随机对照研究旨在比较HLX22联合trastuzumab和化疗与trastuzumab和化疗(有或无pembrolizumab)在HER2阳性晚期胃癌或胃食管交界癌(G/GEJ)患者中的疗效和安全性。研究计划纳入约550名患者,主要终点为无进展生存期(PFS)和总生存期(OS)。该研究旨在为HER2阳性G/GEJ癌患者提供新的治疗选择。
A phase 1, first-in-human study of AMT-676, an anti-CDH17 antibody-drug conjugate, in patients with advanced gastrointestinal tumors.

概述:该Ⅰ期首次人体研究旨在评估抗CDH17抗体药物偶联物(AMT-676)在晚期胃肠道肿瘤患者中的最大耐受剂量(MTD)、推荐Ⅱ期剂量(RP2D)以及安全性、耐受性、药代动力学、药效学、免疫原性和初步疗效。研究纳入了59名患者,结果显示,AMT-676在CLDN18.2阳性胃癌患者中显示出良好的抗肿瘤活性和可管理的安全性,支持其进一步开发。
The anti-STEAP1/PSMA ADC, DXC008: Assessment of anti-tumor efficacy, pharmacokinetic, and toxicity properties.

概述:该研究评估了抗STEAP1/PSMA抗体药物偶联物(DXC008)的抗肿瘤活性、药代动力学和安全性。DXC008在体外和体内模型中显示出良好的抗肿瘤活性和药代动力学特性,且在食蟹猴中耐受性良好。目前正在进行Ⅰ期临床试验,以评估DXC008在晚期实体瘤患者中的安全性、耐受性、药代动力学特征和疗效。
Cadonilimab in combination with ivonescimab and chemotherapy as first-line (1L) therapy in patients with advanced gastric (G) or gastroesophageal junction adenocarcinoma (GEJA).

概述:该Ⅱ期研究旨在评估cadonilimab联合ivonescimab和化疗作为一线治疗方案在晚期胃癌或胃食管交界腺癌(GEJA)患者中的疗效和安全性。研究纳入了21名患者,结果显示,客观反应率(ORR)为75.0%,疾病控制率(DCR)为100%。研究结论表明,该联合治疗方案在晚期G/GEJA患者中具有良好的耐受性和抗肿瘤活性,值得进一步研究。
Final analysis of a multicenter, open-label, phase 2 study evaluating the efficacy and safety of tislelizumab (TIS) in combination with fruquintinib (F) in patients with selected solid tumors.

概述:该Ⅱ期开放标签研究旨在评估tislelizumab联合fruquintinib在晚期实体瘤患者中的疗效和安全性。研究纳入了84名患者,结果显示,客观反应率(ORR)为35.0%(胃癌)和37.5%(微卫星稳定型结直肠癌)。研究结论表明,该联合治疗方案在胃癌和微卫星稳定型结直肠癌患者中显示出中等的抗肿瘤活性和可管理的安全性,值得进一步研究。
afety and efficacy of QLS31905 in patients with advanced solid tumors: Updated data from phase 1 study.

概述:该Ⅰ期研究旨在评估抗CLDN18.2/CD3双特异性抗体QLS31905在晚期实体瘤患者中的安全性、耐受性、药代动力学和初步疗效。研究纳入了79名患者,结果显示,客观反应率(ORR)为18.18%,疾病控制率(DCR)为87.88%,中位无进展生存期(PFS)为4.21个月。研究结论表明,QLS31905在CLDN18.2阳性胃肠道肿瘤患者中显示出良好的抗肿瘤活性和可管理的安全性,值得在Ⅱ期试验中进一步探索。
A phase Ib/IIa study of BAT8010+BAT1006, an anti-HER2 monoclonal antibody-exatecan conjugate combined with an ADCC-enhanced HER2 mAb in patients with advanced solid tumors.

概述:该Ⅰb/Ⅱa期研究旨在评估抗HER2单克隆抗体-依沙替康偶联物(BAT8010)联合增强ADCC活性的HER2单克隆抗体(BAT1006)在晚期实体瘤患者中的疗效和安全性。研究纳入了20名患者,结果显示,客观反应率(ORR)为43.7%,疾病控制率(DCR)为87.5%。研究结论表明,该联合治疗方案在转移性乳腺癌和胃癌患者中显示出良好的耐受性和抗肿瘤活性,值得进一步研究。
Disitamab vedotin (RC48), tislelizumab, and S-1 as first-line therapy for HER2-overexpressing advanced gastric or gastroesophageal junction adenocarcinoma (GC/GEJC): Updated results from the RCTS trial.

概述:该单臂多中心临床试验旨在评估RC48、tislelizumab和S-1作为一线治疗方案在HER2过表达晚期胃癌或胃食管交界腺癌(GC/GEJC)患者中的疗效和安全性。研究纳入了57名患者,结果显示,客观反应率(ORR)为89.4%,中位无进展生存期(PFS)为12.7个月,18个月总生存率(OS)为72.7%。研究结论表明,该联合治疗方案在HER2过表达GC/GEJC患者中显示出良好的抗肿瘤活性和生存获益,支持进一步开展随机对照试验。
fficacy and safety of disitamab vedotin (RC48) combined with camrelizumab and S-1 for neoadjuvant therapy of locally advanced gastric cancer with HER2 overexpression: Preliminary results of a prospective, single-arm, phase II study.

概述:该Ⅱ期单臂研究旨在评估RC48联合camrelizumab和S-1在局部晚期HER2过表达胃癌患者新辅助治疗中的疗效和安全性。研究纳入了32名患者,结果显示,客观反应率(ORR)为80.0%,主要病理反应(MPR)率为45.8%,病理完全缓解(pCR)率为25.0%。研究结论表明,该联合治疗方案在局部晚期可切除HER2过表达胃癌患者中显示出良好的抗肿瘤活性和安全性,值得进一步研究。
Fruquintinib plus sintilimab and SOX as conversion therapy for initially unresectable gastric/gastroesophageal junction adenocarcinoma (GC/GEJC): Updated response and surgical results from a single-arm, phase 2 clinical trial.

概述:该Ⅱ期单臂研究旨在评估fruquintinib联合sintilimab和SOX在初始不可切除胃癌或胃食管交界腺癌(GC/GEJC)患者转化治疗中的疗效和安全性。研究纳入了42名患者,结果显示,客观反应率(ORR)为73.2%,疾病控制率(DCR)为97.6%,R0切除率为100%。研究结论表明,该联合治疗方案在初始不可切除GC/GEJC患者中具有较高的R0切除率和良好的安全性,值得进一步研究。
fficacy and safety of XNW27011, a Claudin 18.2 targeting antibody drug conjugate with topoisomerase 1 inhibitor payload, in patients with Claudin 18.2 positive gastric/gastroesophageal junction cancer: Results from ongoing phase I/II study.

概述:该Ⅰ/Ⅱ期研究旨在评估抗CLDN18.2抗体药物偶联物(XNW27011)在CLDN18.2阳性胃癌或胃食管交界癌(GC/GEJC)患者中的疗效和安全性。研究纳入了116名患者,结果显示,客观反应率(ORR)为46.7%,疾病控制率(DCR)为88.0%。研究结论表明,XNW27011在CLDN18.2阳性GC/GEJC患者中显示出良好的抗肿瘤活性和可管理的安全性,支持其进一步开发。
valuation of the safety and efficacy of sintilimab combined with chemotherapy as neoadjuvant therapy for locally advanced gastric/gastroesophageal junction adenocarcinoma: Short-term results of a multicenter phase II study.

概述:该Ⅱ期多中心研究旨在评估sintilimab联合化疗在局部晚期胃癌或胃食管交界腺癌(LAGC)患者新辅助治疗中的疗效和安全性。研究纳入了26名患者,结果显示,主要病理反应(MPR)率为47.8%,病理完全缓解(pCR)率为30.4%。研究结论表明,sintilimab联合化疗在LAGC患者中显示出良好的抗肿瘤活性和安全性,支持进一步开展大规模随机对照试验。
oadjuvant toripalimab plus CapeOX in patients with locally advanced EBV-positive gastric or esophagogastric junction adenocarcinoma (GC/EGJC): Results from the phase II NICE trial.

概述:该Ⅱ期研究旨在评估toripalimab联合CapeOX在局部晚期EBV阳性胃癌或胃食管交界腺癌(GC/EGJC)患者新辅助治疗中的疗效和安全性。研究纳入了17名患者,结果显示,主要病理反应(MPR)率为37.5%,病理完全缓解(pCR)率为25.0%。研究结论表明,该联合治疗方案在EBV阳性GC/EGJC患者中安全有效,具有中等的MPR和pCR,值得进一步研究。
Updated results of HLX22 plus trastuzumab and XELOX for first-line treatment of human epidermal growth factor receptor 2 (HER2)–positive locally advanced or metastatic gastric/gastroesophageal junction cancer (G/GEJC).

概述:该Ⅱ期研究更新了HLX22联合曲妥珠单抗和XELOX化疗作为HER2阳性晚期胃癌或胃食管交界癌(G/GEJC)一线治疗的疗效和安全性结果。研究纳入了62名患者,中位随访时间为28.5个月。结果显示,联合治疗组的客观反应率(ORR)和无进展生存期(PFS)均优于安慰剂组,且安全性可控。研究结论表明,该联合治疗方案为HER2阳性G/GEJC患者提供了生存获益,且具有可管理的安全性。
First in human phase I study of TQB2103, a Claudin18.2 (CLDN18.2) targeted antibody-drug conjugate (ADC), in patients with advanced solid tumors.

概述:该Ⅰ期首次人体研究评估了靶向CLDN18.2的抗体药物偶联物(TQB2103)在晚期实体瘤患者中的安全性、耐受性、药代动力学和初步抗肿瘤活性。研究纳入了59名患者,结果显示,TQB2103在CLDN18.2阳性胃癌患者中显示出良好的抗肿瘤活性,客观反应率(ORR)为20%,疾病控制率(DCR)为76.7%。研究结论表明,TQB2103具有可管理的安全性,支持其进一步开发。
First-line osemitamab (TST001) plus nivolumab and CAPOX for advanced G/GEJ cancer (TranStar102): Updated results of cohort G from a phase I/IIa study.

概述:该Ⅰ/Ⅱa期研究的队列G更新了osemitamab(TST001)联合nivolumab和CAPOX作为晚期胃癌或胃食管交界癌(G/GEJ)一线治疗的疗效和安全性结果。研究纳入了82名患者,中位随访时间为21.3个月。结果显示,客观反应率(ORR)为55.7%,且在CLDN18.2高/中表达患者中更高。研究结论表明,该联合治疗方案在晚期G/GEJ癌患者中安全且耐受性良好,尤其是对于CLDN18.2高/中表达的患者。
intilimab plus oxaliplatin and capecitabine versus sintilimab plus albumin-bound paclitaxel and capecitabine for advanced unresectable gastric and gastroesophageal junction (GEJ) adenocarcinoma patients: A prospective, randomized, open-label, investigator-initiated phase 2 trial.

概述:该Ⅱ期研究比较了信迪利单抗联合奥沙利铂和卡培他滨与信迪利单抗联合白蛋白结合型紫杉醇和卡培他滨在晚期不可切除胃癌和胃食管交界腺癌(GEJ)患者中的疗效和安全性。研究纳入了39名患者,结果显示两组的客观反应率(ORR)和疾病控制率(DCR)相似,且耐受性良好。研究结论表明,两种方案均显示出相似的疗效和可管理的毒性。
cond-line ASKB589 plus chemotherapy for advanced gastric or gastroesophageal cancers: Results from cohort 5 of a phase I/II study.

概述:该Ⅰ/Ⅱ期研究的第5队列评估了ASKB589联合化疗作为晚期胃癌或胃食管癌二线治疗的疗效和安全性。研究纳入了47名患者,结果显示,客观反应率(ORR)为34.2%,疾病控制率(DCR)为71.1%。研究结论表明,ASKB589联合化疗在CLDN18.2阳性晚期胃癌或胃食管癌患者中显示出良好的抗肿瘤活性和耐受性。
Continuation of serplulimab-based therapy beyond first progression in advanced gastric/gastroesophageal junction (G/GEJ) cancer: Preliminary results from the SCAFIGC trial.

概述:该Ⅱ期研究评估了在晚期胃癌或胃食管交界癌(G/GEJ)患者中,首次进展后继续使用serplulimab为基础的治疗方案的疗效和安全性。研究纳入了53名患者,结果显示,客观反应率(ORR)为52.17%,中位无进展生存期(PFS)为13.73个月。研究结论表明,serplulimab联合化疗在晚期G/GEJ癌患者中显示出良好的疗效和安全性。
HIPEC combined with camrelizumab, paclitaxel and S-1 for conversion therapy in patients with advanced gastric cancer with peritoneal metastasis: A prospective phase II clinical study.

概述:该Ⅱ期研究评估了系统化疗免疫治疗和腹腔热灌注化疗(HIPEC)联合细胞减灭术(CRS)在胃癌腹膜转移患者中的疗效和安全性。研究纳入了48名患者,结果显示,CRS组的R0切除率为90.3%,中位总生存期(OS)显著优于姑息治疗组。研究结论表明,该联合治疗方案安全可行,可能改善有限腹膜转移胃癌患者的预后。
The appropriate therapeutic sequence with angiogenesis inhibitor and chemotherapy in patients with advanced gastric or gastroesophageal junction adenocarcinoma: Exploratory analysis from the phase 3 FRUTIGA study.

概述:该Ⅲ期FRUTIGA研究的事后分析旨在探索晚期胃癌或胃食管交界腺癌患者中,抗血管生成抑制剂和化疗的最佳治疗顺序。研究纳入了117名患者,结果显示,与化疗后使用抗血管生成抑制剂相比,先使用抗血管生成抑制剂后化疗的治疗顺序显示出更好的生存获益。研究结论表明,该治疗顺序可能为晚期胃癌或胃食管交界腺癌患者提供更好的临床结果。
Camrelizumab plus albumin-bound paclitaxel and S-1 as first-line treatment of HER-2 negative unresectable locally advanced or advanced gastric and gastroesophageal junction adenocarcinoma: A phase II clinical trial.

概述:该Ⅱ期研究评估了卡瑞利珠单抗联合白蛋白结合型紫杉醇和S-1作为一线治疗方案在HER2阴性不可切除局部晚期或晚期胃癌和胃食管交界腺癌患者中的疗效和安全性。研究纳入了47名患者,结果显示,客观反应率(ORR)为67.5%,中位无进展生存期(PFS)为7.8个月,中位总生存期(OS)为23.8个月。研究结论表明,该联合治疗方案在HER2阴性晚期胃癌和胃食管交界腺癌患者中显示出良好的抗肿瘤活性。
arT cell combined with PD-1 blockade and SOX as first-line treatment for patients with advanced gastric/gastroesophageal junction adenocarcinoma.

概述:该研究评估了SmarT细胞联合PD-1阻断和SOX方案作为晚期胃癌或胃食管交界腺癌一线治疗的疗效和安全性。研究纳入了50名患者,结果显示,联合治疗组的客观反应率(ORR)为66%,疾病控制率(DCR)为94%。研究结论表明,SmarT细胞联合PD-1阻断和SOX方案在晚期胃癌或胃食管交界腺癌患者中显示出优越的ORR和PFS获益,且安全性可接受。
A dose escalation and cohort expansion phase I/IIa study of ACR246, an innovative 5T4-antibody drug conjugate (ADC), in patients with advanced solid tumors.

概述:该Ⅰ/Ⅱa期研究评估了创新5T4抗体药物偶联物(ACR246)在晚期实体瘤患者中的剂量递增和队列扩展。研究纳入了77名患者,结果显示,ACR246在多种实体瘤中显示出良好的抗肿瘤活性和可管理的安全性。研究结论表明,ACR246具有进一步开发的潜力,尤其是在5T4阳性实体瘤患者中。
A first-in-human clinical study of 9MW2921, a novel TROP-2 antibody-drug conjugate (ADC), in patients with advanced solid tumors.

概述:该首次人体研究评估了新型TROP-2抗体药物偶联物(9MW2921)在晚期实体瘤患者中的疗效和安全性。研究纳入了39名患者,结果显示,9MW2921在多种实体瘤中显示出良好的抗肿瘤活性,客观反应率(ORR)为42.1%。研究结论表明,9MW2921具有可接受的耐受性和良好的抗肿瘤活性,支持其进一步开发。
reoperative PD-1 inhibitor (tislelizumab) plus SOX for locally advanced gastric or gastro-oesophageal junction cancer: Results from a single-arm, phase II trial.

概述:该Ⅱ期单臂研究评估了PD-1抑制剂(替雷利珠单抗)联合SOX方案在局部晚期胃癌或胃食管交界癌患者新辅助治疗中的疗效和安全性。研究纳入了31名患者,结果显示,主要病理反应(MPR)率为37.0%,病理完全缓解(pCR)率为18.5%。研究结论表明,替雷利珠单抗联合SOX方案在局部晚期可切除胃癌或胃食管交界癌患者中显示出良好的抗肿瘤活性和可控的安全性,可能成为一种有前景的治疗选择。
总结
2025年ASCO会议上,中国学者在胃癌抗体治疗领域取得了令人瞩目的成果。这些研究不仅展示了中国在胃癌治疗领域的创新能力,也为全球胃癌治疗提供了新的思路和方法。通过抗体药物与化疗、免疫治疗等的联合应用,研究者们在提高患者生存率、改善治疗耐受性方面取得了显著进展;这些研究不仅为胃癌患者带来了新的治疗选择,也为未来的研究方向提供了重要指引。随着更多创新性抗体药物的开发和临床试验的推进,胃癌治疗有望迎来新的突破,为患者带来更多的生存希望。
国家癌症中心最新发布的数据显示,我国胃癌的年发病人数超过35万,位列所有恶性肿瘤第5位;死亡人数超过26万人,位列恶性肿瘤第3位。我国胃癌患者大约占全球40%——这意味着,我每天有近千人被确诊为胃癌。更严峻的是,大部分患者确诊时已到晚期,错过最佳治疗窗口。
在2025年美国临床肿瘤学会(ASCO)年会上,中国学者在胃癌治疗领域展示了多项数据,尤其是抗体药物及其联合治疗方案的研究成果备受瞩目。近年来,随着免疫治疗、靶向治疗等新兴疗法的不断发展,胃癌的治疗格局正在发生深刻变革。本次ASCO会议上,中国研究团队展示的多项创新性抗体药物的研究成果,不仅涵盖了HER2、CLDN18.2等经典靶点,还探索了新兴靶点如TROP-2、STEAP1等的应用潜力。这些研究不仅为胃癌患者带来了新的治疗希望,也为全球胃癌治疗领域提供了重要的参考和借鉴。
2025ASCO中国胃癌抗体类摘要汇总

RC48-ADC combined with radiotherapy and immunotherapy as salvage therapy for advanced solid tumors with HER2 expression: A multicenter, phase II trial.

概述:该多中心Ⅱ期试验旨在评估RC48-ADC联合放疗和免疫治疗在HER2表达的晚期实体瘤患者中的疗效和安全性。研究纳入了52名患者,包括妇科肿瘤、胰腺癌和胃癌等。结果显示,总体客观反应率(ORR)为36.5%,中位无进展生存期(PFS)为5.9个月,中位总生存期(OS)为14.3个月。治疗相关不良事件大多为轻度。研究结论表明,这种联合疗法在HER2表达的晚期实体瘤患者中显示出良好的疗效和可管理的安全性,有望成为一种有效的挽救治疗选择。
A multiregional, randomized, controlled, open-label, phase 3 study of the anti-claudin18.2 (CLDN18.2) antibody-drug conjugate (ADC) arcotatug tavatecan (IBI343) in gastric or gastroesophageal junction adenocarcinoma (G/GEJA): Trial in progress.

概述:这项多区域、随机、对照、开放标签的Ⅲ期研究旨在评估抗CLDN18.2抗体药物偶联物(ADC)arcotatug tavatecan(IBI343)在胃或胃食管交界腺癌(G/GEJA)患者中的疗效和安全性。研究计划纳入450名患者,主要纳入标准包括局部晚期不可切除或转移性G/GEJA、CLDN18.2阳性(IHC膜染色强度≥2+,≥75%肿瘤细胞)等。主要终点为无进展生存期(PFS)和总生存期(OS)。研究正在进行中,旨在为CLDN18.2阳性G/GEJA患者提供新的治疗选择。
fficacy and safety of LM-302 (anti-claudin 18.2 ADC) in combination with anti-PD-1 therapy for advanced gastric, gastroesophageal junction cancer and esophageal adenocarcinoma: Early-phase study results.

概述:该早期研究评估了抗CLDN18.2 ADC(LM-302)联合抗PD-1疗法(toripalimab)作为一线治疗方案在晚期胃癌、胃食管交界癌和食管腺癌患者中的疗效和安全性。研究纳入了43名患者,结果显示联合治疗的客观反应率(ORR)为65.9%,疾病控制率(DCR)为85.4%。在CLDN18.2高表达(IHC 2+/3+)的胃癌患者中,ORR为71.9%。研究结论表明,LM-302联合toripalimab在CLDN18.2阳性患者中显示出良好的抗肿瘤活性和可管理的安全性,支持进一步开展大规模临床试验。
HER2 expression dynamics and prognostic significance in the treatment of gastric cancer.

概述:该研究探讨了胃癌治疗过程中HER2表达的变化及其对预后的影响。研究纳入了274名胃癌患者,分析了治疗前后HER2免疫组化(IHC)结果。结果显示,HER2表达变化率为42.7%,低一致性(Kappa=0.179)。在接受抗HER2治疗的患者中,HER2表达变化率更高,主要表现为HER2减少。研究结论表明,HER2表达在胃癌治疗过程中频繁变化,尤其在免疫治疗和靶向治疗后,与较差的生存结果相关,动态HER2检测有助于指导胃癌的精准治疗。
A pooled analysis of JSKN003, a biparatopic anti-HER2 antibody conjugate (ADC), in patients with advanced HER2-overexpressing (IHC 3+) gastrointestinal tumors.

概述:该研究对JSKN003(一种双特异性抗HER2抗体药物偶联物)在HER2过表达(IHC 3+)胃肠道肿瘤患者中的疗效和安全性进行了汇总分析。研究纳入了40名患者,结果显示,整体客观反应率(ORR)为66.7%,疾病控制率(DCR)为94.7%。在胃癌/胃食管交界癌患者中,ORR为68.2%,中位无进展生存期(PFS)为9.59个月。研究结论表明,JSKN003在经多线治疗的患者中显示出良好的抗肿瘤活性和可管理的安全性,支持其进一步开发。
A randomized, double-blinded, international phase III trial comparing HLX22 in combination with trastuzumab and chemotherapy versus trastuzumab and chemotherapy with or without pembrolizumab for first-line treatment for HER2-positive locally advanced or metastatic G/GEJ cancer.

概述:该国际Ⅲ期随机对照研究旨在比较HLX22联合trastuzumab和化疗与trastuzumab和化疗(有或无pembrolizumab)在HER2阳性晚期胃癌或胃食管交界癌(G/GEJ)患者中的疗效和安全性。研究计划纳入约550名患者,主要终点为无进展生存期(PFS)和总生存期(OS)。该研究旨在为HER2阳性G/GEJ癌患者提供新的治疗选择。
A phase 1, first-in-human study of AMT-676, an anti-CDH17 antibody-drug conjugate, in patients with advanced gastrointestinal tumors.

概述:该Ⅰ期首次人体研究旨在评估抗CDH17抗体药物偶联物(AMT-676)在晚期胃肠道肿瘤患者中的最大耐受剂量(MTD)、推荐Ⅱ期剂量(RP2D)以及安全性、耐受性、药代动力学、药效学、免疫原性和初步疗效。研究纳入了59名患者,结果显示,AMT-676在CLDN18.2阳性胃癌患者中显示出良好的抗肿瘤活性和可管理的安全性,支持其进一步开发。
The anti-STEAP1/PSMA ADC, DXC008: Assessment of anti-tumor efficacy, pharmacokinetic, and toxicity properties.

概述:该研究评估了抗STEAP1/PSMA抗体药物偶联物(DXC008)的抗肿瘤活性、药代动力学和安全性。DXC008在体外和体内模型中显示出良好的抗肿瘤活性和药代动力学特性,且在食蟹猴中耐受性良好。目前正在进行Ⅰ期临床试验,以评估DXC008在晚期实体瘤患者中的安全性、耐受性、药代动力学特征和疗效。
Cadonilimab in combination with ivonescimab and chemotherapy as first-line (1L) therapy in patients with advanced gastric (G) or gastroesophageal junction adenocarcinoma (GEJA).

概述:该Ⅱ期研究旨在评估cadonilimab联合ivonescimab和化疗作为一线治疗方案在晚期胃癌或胃食管交界腺癌(GEJA)患者中的疗效和安全性。研究纳入了21名患者,结果显示,客观反应率(ORR)为75.0%,疾病控制率(DCR)为100%。研究结论表明,该联合治疗方案在晚期G/GEJA患者中具有良好的耐受性和抗肿瘤活性,值得进一步研究。
Final analysis of a multicenter, open-label, phase 2 study evaluating the efficacy and safety of tislelizumab (TIS) in combination with fruquintinib (F) in patients with selected solid tumors.

概述:该Ⅱ期开放标签研究旨在评估tislelizumab联合fruquintinib在晚期实体瘤患者中的疗效和安全性。研究纳入了84名患者,结果显示,客观反应率(ORR)为35.0%(胃癌)和37.5%(微卫星稳定型结直肠癌)。研究结论表明,该联合治疗方案在胃癌和微卫星稳定型结直肠癌患者中显示出中等的抗肿瘤活性和可管理的安全性,值得进一步研究。
afety and efficacy of QLS31905 in patients with advanced solid tumors: Updated data from phase 1 study.

概述:该Ⅰ期研究旨在评估抗CLDN18.2/CD3双特异性抗体QLS31905在晚期实体瘤患者中的安全性、耐受性、药代动力学和初步疗效。研究纳入了79名患者,结果显示,客观反应率(ORR)为18.18%,疾病控制率(DCR)为87.88%,中位无进展生存期(PFS)为4.21个月。研究结论表明,QLS31905在CLDN18.2阳性胃肠道肿瘤患者中显示出良好的抗肿瘤活性和可管理的安全性,值得在Ⅱ期试验中进一步探索。
A phase Ib/IIa study of BAT8010+BAT1006, an anti-HER2 monoclonal antibody-exatecan conjugate combined with an ADCC-enhanced HER2 mAb in patients with advanced solid tumors.

概述:该Ⅰb/Ⅱa期研究旨在评估抗HER2单克隆抗体-依沙替康偶联物(BAT8010)联合增强ADCC活性的HER2单克隆抗体(BAT1006)在晚期实体瘤患者中的疗效和安全性。研究纳入了20名患者,结果显示,客观反应率(ORR)为43.7%,疾病控制率(DCR)为87.5%。研究结论表明,该联合治疗方案在转移性乳腺癌和胃癌患者中显示出良好的耐受性和抗肿瘤活性,值得进一步研究。
Disitamab vedotin (RC48), tislelizumab, and S-1 as first-line therapy for HER2-overexpressing advanced gastric or gastroesophageal junction adenocarcinoma (GC/GEJC): Updated results from the RCTS trial.

概述:该单臂多中心临床试验旨在评估RC48、tislelizumab和S-1作为一线治疗方案在HER2过表达晚期胃癌或胃食管交界腺癌(GC/GEJC)患者中的疗效和安全性。研究纳入了57名患者,结果显示,客观反应率(ORR)为89.4%,中位无进展生存期(PFS)为12.7个月,18个月总生存率(OS)为72.7%。研究结论表明,该联合治疗方案在HER2过表达GC/GEJC患者中显示出良好的抗肿瘤活性和生存获益,支持进一步开展随机对照试验。
fficacy and safety of disitamab vedotin (RC48) combined with camrelizumab and S-1 for neoadjuvant therapy of locally advanced gastric cancer with HER2 overexpression: Preliminary results of a prospective, single-arm, phase II study.

概述:该Ⅱ期单臂研究旨在评估RC48联合camrelizumab和S-1在局部晚期HER2过表达胃癌患者新辅助治疗中的疗效和安全性。研究纳入了32名患者,结果显示,客观反应率(ORR)为80.0%,主要病理反应(MPR)率为45.8%,病理完全缓解(pCR)率为25.0%。研究结论表明,该联合治疗方案在局部晚期可切除HER2过表达胃癌患者中显示出良好的抗肿瘤活性和安全性,值得进一步研究。
Fruquintinib plus sintilimab and SOX as conversion therapy for initially unresectable gastric/gastroesophageal junction adenocarcinoma (GC/GEJC): Updated response and surgical results from a single-arm, phase 2 clinical trial.

概述:该Ⅱ期单臂研究旨在评估fruquintinib联合sintilimab和SOX在初始不可切除胃癌或胃食管交界腺癌(GC/GEJC)患者转化治疗中的疗效和安全性。研究纳入了42名患者,结果显示,客观反应率(ORR)为73.2%,疾病控制率(DCR)为97.6%,R0切除率为100%。研究结论表明,该联合治疗方案在初始不可切除GC/GEJC患者中具有较高的R0切除率和良好的安全性,值得进一步研究。
fficacy and safety of XNW27011, a Claudin 18.2 targeting antibody drug conjugate with topoisomerase 1 inhibitor payload, in patients with Claudin 18.2 positive gastric/gastroesophageal junction cancer: Results from ongoing phase I/II study.

概述:该Ⅰ/Ⅱ期研究旨在评估抗CLDN18.2抗体药物偶联物(XNW27011)在CLDN18.2阳性胃癌或胃食管交界癌(GC/GEJC)患者中的疗效和安全性。研究纳入了116名患者,结果显示,客观反应率(ORR)为46.7%,疾病控制率(DCR)为88.0%。研究结论表明,XNW27011在CLDN18.2阳性GC/GEJC患者中显示出良好的抗肿瘤活性和可管理的安全性,支持其进一步开发。
valuation of the safety and efficacy of sintilimab combined with chemotherapy as neoadjuvant therapy for locally advanced gastric/gastroesophageal junction adenocarcinoma: Short-term results of a multicenter phase II study.

概述:该Ⅱ期多中心研究旨在评估sintilimab联合化疗在局部晚期胃癌或胃食管交界腺癌(LAGC)患者新辅助治疗中的疗效和安全性。研究纳入了26名患者,结果显示,主要病理反应(MPR)率为47.8%,病理完全缓解(pCR)率为30.4%。研究结论表明,sintilimab联合化疗在LAGC患者中显示出良好的抗肿瘤活性和安全性,支持进一步开展大规模随机对照试验。
oadjuvant toripalimab plus CapeOX in patients with locally advanced EBV-positive gastric or esophagogastric junction adenocarcinoma (GC/EGJC): Results from the phase II NICE trial.

概述:该Ⅱ期研究旨在评估toripalimab联合CapeOX在局部晚期EBV阳性胃癌或胃食管交界腺癌(GC/EGJC)患者新辅助治疗中的疗效和安全性。研究纳入了17名患者,结果显示,主要病理反应(MPR)率为37.5%,病理完全缓解(pCR)率为25.0%。研究结论表明,该联合治疗方案在EBV阳性GC/EGJC患者中安全有效,具有中等的MPR和pCR,值得进一步研究。
Updated results of HLX22 plus trastuzumab and XELOX for first-line treatment of human epidermal growth factor receptor 2 (HER2)–positive locally advanced or metastatic gastric/gastroesophageal junction cancer (G/GEJC).

概述:该Ⅱ期研究更新了HLX22联合曲妥珠单抗和XELOX化疗作为HER2阳性晚期胃癌或胃食管交界癌(G/GEJC)一线治疗的疗效和安全性结果。研究纳入了62名患者,中位随访时间为28.5个月。结果显示,联合治疗组的客观反应率(ORR)和无进展生存期(PFS)均优于安慰剂组,且安全性可控。研究结论表明,该联合治疗方案为HER2阳性G/GEJC患者提供了生存获益,且具有可管理的安全性。
First in human phase I study of TQB2103, a Claudin18.2 (CLDN18.2) targeted antibody-drug conjugate (ADC), in patients with advanced solid tumors.

概述:该Ⅰ期首次人体研究评估了靶向CLDN18.2的抗体药物偶联物(TQB2103)在晚期实体瘤患者中的安全性、耐受性、药代动力学和初步抗肿瘤活性。研究纳入了59名患者,结果显示,TQB2103在CLDN18.2阳性胃癌患者中显示出良好的抗肿瘤活性,客观反应率(ORR)为20%,疾病控制率(DCR)为76.7%。研究结论表明,TQB2103具有可管理的安全性,支持其进一步开发。
First-line osemitamab (TST001) plus nivolumab and CAPOX for advanced G/GEJ cancer (TranStar102): Updated results of cohort G from a phase I/IIa study.

概述:该Ⅰ/Ⅱa期研究的队列G更新了osemitamab(TST001)联合nivolumab和CAPOX作为晚期胃癌或胃食管交界癌(G/GEJ)一线治疗的疗效和安全性结果。研究纳入了82名患者,中位随访时间为21.3个月。结果显示,客观反应率(ORR)为55.7%,且在CLDN18.2高/中表达患者中更高。研究结论表明,该联合治疗方案在晚期G/GEJ癌患者中安全且耐受性良好,尤其是对于CLDN18.2高/中表达的患者。
intilimab plus oxaliplatin and capecitabine versus sintilimab plus albumin-bound paclitaxel and capecitabine for advanced unresectable gastric and gastroesophageal junction (GEJ) adenocarcinoma patients: A prospective, randomized, open-label, investigator-initiated phase 2 trial.

概述:该Ⅱ期研究比较了信迪利单抗联合奥沙利铂和卡培他滨与信迪利单抗联合白蛋白结合型紫杉醇和卡培他滨在晚期不可切除胃癌和胃食管交界腺癌(GEJ)患者中的疗效和安全性。研究纳入了39名患者,结果显示两组的客观反应率(ORR)和疾病控制率(DCR)相似,且耐受性良好。研究结论表明,两种方案均显示出相似的疗效和可管理的毒性。
cond-line ASKB589 plus chemotherapy for advanced gastric or gastroesophageal cancers: Results from cohort 5 of a phase I/II study.

概述:该Ⅰ/Ⅱ期研究的第5队列评估了ASKB589联合化疗作为晚期胃癌或胃食管癌二线治疗的疗效和安全性。研究纳入了47名患者,结果显示,客观反应率(ORR)为34.2%,疾病控制率(DCR)为71.1%。研究结论表明,ASKB589联合化疗在CLDN18.2阳性晚期胃癌或胃食管癌患者中显示出良好的抗肿瘤活性和耐受性。
Continuation of serplulimab-based therapy beyond first progression in advanced gastric/gastroesophageal junction (G/GEJ) cancer: Preliminary results from the SCAFIGC trial.

概述:该Ⅱ期研究评估了在晚期胃癌或胃食管交界癌(G/GEJ)患者中,首次进展后继续使用serplulimab为基础的治疗方案的疗效和安全性。研究纳入了53名患者,结果显示,客观反应率(ORR)为52.17%,中位无进展生存期(PFS)为13.73个月。研究结论表明,serplulimab联合化疗在晚期G/GEJ癌患者中显示出良好的疗效和安全性。
HIPEC combined with camrelizumab, paclitaxel and S-1 for conversion therapy in patients with advanced gastric cancer with peritoneal metastasis: A prospective phase II clinical study.

概述:该Ⅱ期研究评估了系统化疗免疫治疗和腹腔热灌注化疗(HIPEC)联合细胞减灭术(CRS)在胃癌腹膜转移患者中的疗效和安全性。研究纳入了48名患者,结果显示,CRS组的R0切除率为90.3%,中位总生存期(OS)显著优于姑息治疗组。研究结论表明,该联合治疗方案安全可行,可能改善有限腹膜转移胃癌患者的预后。
The appropriate therapeutic sequence with angiogenesis inhibitor and chemotherapy in patients with advanced gastric or gastroesophageal junction adenocarcinoma: Exploratory analysis from the phase 3 FRUTIGA study.

概述:该Ⅲ期FRUTIGA研究的事后分析旨在探索晚期胃癌或胃食管交界腺癌患者中,抗血管生成抑制剂和化疗的最佳治疗顺序。研究纳入了117名患者,结果显示,与化疗后使用抗血管生成抑制剂相比,先使用抗血管生成抑制剂后化疗的治疗顺序显示出更好的生存获益。研究结论表明,该治疗顺序可能为晚期胃癌或胃食管交界腺癌患者提供更好的临床结果。
Camrelizumab plus albumin-bound paclitaxel and S-1 as first-line treatment of HER-2 negative unresectable locally advanced or advanced gastric and gastroesophageal junction adenocarcinoma: A phase II clinical trial.

概述:该Ⅱ期研究评估了卡瑞利珠单抗联合白蛋白结合型紫杉醇和S-1作为一线治疗方案在HER2阴性不可切除局部晚期或晚期胃癌和胃食管交界腺癌患者中的疗效和安全性。研究纳入了47名患者,结果显示,客观反应率(ORR)为67.5%,中位无进展生存期(PFS)为7.8个月,中位总生存期(OS)为23.8个月。研究结论表明,该联合治疗方案在HER2阴性晚期胃癌和胃食管交界腺癌患者中显示出良好的抗肿瘤活性。
arT cell combined with PD-1 blockade and SOX as first-line treatment for patients with advanced gastric/gastroesophageal junction adenocarcinoma.

概述:该研究评估了SmarT细胞联合PD-1阻断和SOX方案作为晚期胃癌或胃食管交界腺癌一线治疗的疗效和安全性。研究纳入了50名患者,结果显示,联合治疗组的客观反应率(ORR)为66%,疾病控制率(DCR)为94%。研究结论表明,SmarT细胞联合PD-1阻断和SOX方案在晚期胃癌或胃食管交界腺癌患者中显示出优越的ORR和PFS获益,且安全性可接受。
A dose escalation and cohort expansion phase I/IIa study of ACR246, an innovative 5T4-antibody drug conjugate (ADC), in patients with advanced solid tumors.

概述:该Ⅰ/Ⅱa期研究评估了创新5T4抗体药物偶联物(ACR246)在晚期实体瘤患者中的剂量递增和队列扩展。研究纳入了77名患者,结果显示,ACR246在多种实体瘤中显示出良好的抗肿瘤活性和可管理的安全性。研究结论表明,ACR246具有进一步开发的潜力,尤其是在5T4阳性实体瘤患者中。
A first-in-human clinical study of 9MW2921, a novel TROP-2 antibody-drug conjugate (ADC), in patients with advanced solid tumors.

概述:该首次人体研究评估了新型TROP-2抗体药物偶联物(9MW2921)在晚期实体瘤患者中的疗效和安全性。研究纳入了39名患者,结果显示,9MW2921在多种实体瘤中显示出良好的抗肿瘤活性,客观反应率(ORR)为42.1%。研究结论表明,9MW2921具有可接受的耐受性和良好的抗肿瘤活性,支持其进一步开发。
reoperative PD-1 inhibitor (tislelizumab) plus SOX for locally advanced gastric or gastro-oesophageal junction cancer: Results from a single-arm, phase II trial.

概述:该Ⅱ期单臂研究评估了PD-1抑制剂(替雷利珠单抗)联合SOX方案在局部晚期胃癌或胃食管交界癌患者新辅助治疗中的疗效和安全性。研究纳入了31名患者,结果显示,主要病理反应(MPR)率为37.0%,病理完全缓解(pCR)率为18.5%。研究结论表明,替雷利珠单抗联合SOX方案在局部晚期可切除胃癌或胃食管交界癌患者中显示出良好的抗肿瘤活性和可控的安全性,可能成为一种有前景的治疗选择。
总结
2025年ASCO会议上,中国学者在胃癌抗体治疗领域取得了令人瞩目的成果。这些研究不仅展示了中国在胃癌治疗领域的创新能力,也为全球胃癌治疗提供了新的思路和方法。通过抗体药物与化疗、免疫治疗等的联合应用,研究者们在提高患者生存率、改善治疗耐受性方面取得了显著进展;这些研究不仅为胃癌患者带来了新的治疗选择,也为未来的研究方向提供了重要指引。随着更多创新性抗体药物的开发和临床试验的推进,胃癌治疗有望迎来新的突破,为患者带来更多的生存希望。


